Примеры решения задач.
Пример №1. Найти изменение DS энтропии при нагревании воды массой m=100 г от температуры t1=0°C до температуры t2=100 °С и последующем превращении воды в пар той же температуры.
Решение. Найдем отдельно изменение энтропии DS' при нагревании воды и изменение энтропии DS" при превращении ее в пар. Полное изменение энтропии выразится суммой DS' и DS".
Как известно, изменение энтропии выражается общей формулой
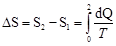 (1)
(1)
При бесконечно малом изменении dT температуры нагреваемого тела затрачивается количество теплоты 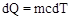 , где m — масса тела; с — его удельная теплоемкость. Подставив выражение dQ в равенство (1), найдем формулу для вычисления изменения энтропии при нагревании воды:
, где m — масса тела; с — его удельная теплоемкость. Подставив выражение dQ в равенство (1), найдем формулу для вычисления изменения энтропии при нагревании воды:
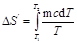 .
.
Вынесем за знак интеграла постоянные величины и произведем интегрирование, тогда получим
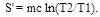
После вычислений найдем 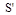 =132 Дж/К.
=132 Дж/К.
При вычислении по формуле (1) изменения энтропии во время превращения воды в пар той же температуры постоянная температуpa T 'выносится за знак интеграла. Вычислив интеграл, найдем
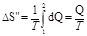 (2)
(2)
где Q — количество теплоты, переданное при превращении нагретой воды в пар той же температуры.
Подставив в равенство (2) выражение количества теплоты Q=lm, где l — удельная теплота парообразования, получим
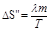 (3)
(3)
Произведя вычисления по формуле (3), найдем
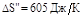
Полное изменение энтропии при нагревании воды и последующем превращении ее в пар 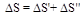
Пример №2. Определить изменение DS энтропии при изотермическом расширении кислорода массой m=10 г от объема V1=25 л до объема V2=100 л.
Решение. Так как процесс изотермический, то в общем выражении энтропии 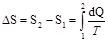 температуру выносят за знак интеграла. Выполнив это, получим
температуру выносят за знак интеграла. Выполнив это, получим
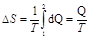 (1)
(1)
Количество теплоты, полученное газом, найдем по первому началу термодинамики: 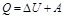 . Для изотермического процесса
. Для изотермического процесса 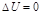 . (2)
. (2)
Работа 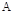 для этого процесса определяется по формуле
для этого процесса определяется по формуле
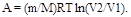 (3)
(3)
С учетом (2) и (3) равенство (1) примет вид
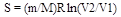 . (4)
. (4)
Подставив в (4) числовые значения и произведя вычисления, получим
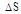 =(10×10-3/(32×10-3)) ×8,31 ln(100×10-3/(25×10-3)) Дж/К=3,60 Дж/К.
=(10×10-3/(32×10-3)) ×8,31 ln(100×10-3/(25×10-3)) Дж/К=3,60 Дж/К.