Глава 2
Расчет физико-химических свойств и состава углеводородных газов
2.1 Особенности расчета физико-химических свойств газовых смесей. Плотность газов
Общие свойства газовых смесей. По сравнению с молекулами жидкости молекулы газов удалены друг от друга на неизмеримо большие расстояния, чем их собственные размеры. С этим связаны некоторые особые свойства газов, например способность к сжатию со значительным изменением объема, заметное повышение давления с ростом температуры и т.д. Поведение газообразных веществ достаточно полно объясняет кинетическая теория газов, основу которой составляют законы газового состояния Бойля-Мариотта, Гей-Люссака и Шарля [10]. Эти законы могут быть выражены объединенным уравнением (законом) Клайперона-Менделеева
pV=NRT. (2.1)
Здесь R – универсальная газовая постоянная, значение которой зависит от выбора системы единиц. Так, в СИ, где давление выражено в паскалях, объем – в кубических метрах и температура – в кельвинах, для одного моля газа R=8,314 Дж/(моль×К).
Зависимость между парциальными давлениями pi компонентов газовой смеси и общим давлением p в системе устанавливается законом Дальтона
p=p1+p2+…+pn=Spi,
где  .
.
В соответствии с законом Рауля в условиях равновесия можно записать 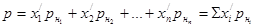
или (см. уравнением 1.10) 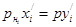 .
.
Приведенные выше законы полностью справедливы для идеальных газов. Углеводородные газы и нефтяные пары можно приближенно считать идеальными газами, особенно при невысоких давлениях. При расчетах допустимо использовать все названные законы. Об особых случаях расчета будет сказано ниже.
Напомним, что в приложении к газам существуют нормальные и стандартные условия, которые при одном и том же давлении (101,3 кПа) отличаются только температурой (273 К и 293 К, соответственно для нормальных и стандартных условий). Параметры, характеризующие состояние газа в нормальных условиях, имеют индекс 0 (V0, p0, T0), в стандартных – 20 (V20, p20, T20). Приведение объема газа к нормальным или стандартным условиям легко осуществляется по формулам:


Пример 2.1 В баллоне вместимостью 0,2 м3 при давлении 3×105 Па и температуре 20°С находится газовая смесь, средняя молярная масса которой М=48 г/моль. Определить массу газовой смеси.
Решение. Зная, что число молей равно отношению массы вещества к его молярной массе, запишем уравнение Клапейрона-Менделеева в виде pV=(m/M)RT. Выразим массу газа m: m=pVM/RT. Подставив известные значения параметров, определим массу газа:
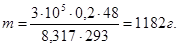
Пример 2.2 Газ при давлении 230 кПа и температуре 46°С занимает объем 1,5 м3. Привести объем газа к нормальным условиям.
Решение. Нормальный объем газа определим, имея в виду, что Т0=273 К и р0=101,3 кПа,

Плотность. Как и для жидкости, плотность газа может быть выражена абсолютным или относительным значением. Абсолютная плотность газа равна его массе в единице объема, в СИ она выражается в килограммах на кубический метр (кг/м3). Величину, обратную плотности, называют удельным объемом и измеряют в кубических метрах на килограмм (м3/кг).
При определении относительной плотности газов и паров нефтепродуктов в качестве стандартного вещества берется воздух при нормальных условиях (Т=273 К, r=101,3 кПа). Отношение массы газа m к массе воздуха mв, взятых в одинаковых объемах и при тех же температуре и давлении, дает относительную плотность газа: 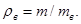
Масса любого идеального газа при нормальных условиях равна его молярной массе, поделенной на объем, занимаемый одним молем, т.е.  , где
, где 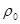 - плотность газа при нормальных условиях.
- плотность газа при нормальных условиях.
Тогда для относительной плотности газа по воздуху можно записать  – молярная масса воздуха, г/моль.
– молярная масса воздуха, г/моль.
Если записать уравнение Клапейрона-Менделеева в виде m/V=pM/RТ, нетрудно увидеть, что левая часть представляет собой плотность газа r, т.е.
r=rM/RТ. (2.2)
Формула (2.2) дает возможность подсчитать истинную плотность газа при любых температуре и давлении.
Существует другая модификация уравнения Клапейрона-Менделеева, также позволяющая определить плотность газа при любых условиях:
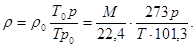 (2.3)
(2.3)
Результаты, получаемые по формулам (2.2) и (2.3), одинаковы. Плотность некоторых индивидуальных газов в зависимости от изменения температуры можно, кроме того, найти по графикам и таблицам [11].
Пример 2.3. Относительная плотность газа равна 1,10. Определить его абсолютную плотность при 150°С и 750 кПа.
Решение. Найдем молярную массу газа:
М=1,1·28,9=31,8 кг/моль.
Абсолютную плотность газа определим по формуле (2.3):
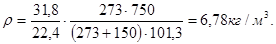
Тот же ответ получим, воспользовавшись формулой (2.2), однако в этом случае нужно выразить М в килограммах на моль (умножить на 10-3), чтобы привести в соответствие с единицами измерения универсальной газовой постоянной.
Плотность газовой смеси может быть подсчитана по формулам для жидкой смеси (см.§1.2). Учитывая, что для газов объемные доли равны молярным, в приложении к газовой смеси можно записать 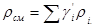
Значения плотности и некоторых других свойств индивидуальных газов приведены в прил.16.
ЗАДАЧИ
2.1. Определить вместимость баллона, в который можно закачать
6 м3 газа, измеренного при нормальных условиях. Максимальное давление в баллоне 15 МПа.
2.2. Во сколько раз возрастет давление в герметичном газовом резервуаре, если температура окружающего воздуха повысится с 10 до 24°С?
2.3. При давлении 360 кПа и температуре 400 К газ занимает объем 1,2 м3. Найти число молей газа.
2.4. Газ в количестве 9 кг находится в сосуде вместимостью 3 м3 при 298 К и 462 кПа. Найти молярную массу газа.
2.5. Определить объем газа при нормальных условиях, если при температуре 120°С и давлении 790 кПа его объем равен 16,3 м3.
2.6. Используя уравнение (2.1), найти плотность метана и этана при нормальных условиях.
2.7. Определить плотность пропана при 150 кПа и 80°С.
2.8. Средняя молярная масса водородсодержащего газа, применяемого в процессе каталитического риформинга, равна 3,5 г/моль. Рассчитать плотность этого газа при 450°С и 3 МПа.
2.9. Газовая смесь состоит из метана и водорода, парциальные давления которых равны 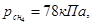
 Определить содержание (в молярных долях) компонентов смеси.
Определить содержание (в молярных долях) компонентов смеси.
2.10. Рассчитать плотность газовой смеси, состоящей из 14 кг пропана, 11 кг этана и 8 кг этилена. Плотности индивидуальных газов взять в прил.16.
2.11. Смешали 3 моля пропана и 7 молей пропилена. Какова плотность полученной смеси?
2.12. Относительная плотность газовой смеси по воздуху равна 1,3. При какой температуре абсолютная плотность станет равной 7 кг/м3, если давление в системе составляет 640 кПа?
2.13. Природный газ Астраханского происхождения имеет следующий состав (в объемных процентах): СН4 – 47,48; С2Н6 – 1,92; С3Н8 – 0,93; С4Н10 – 0,56; С5Н12 –3,08; N2 –1,98; СО2 – 21,55; Н2S – 22,5. Определить плотность газа при нормальных условиях.