Внешний механизм
Активация тканевым фактором
| +Калликреин ВМК |
| XII |
| Тромбомодулин I у,., | тромбин Протеин С±^_Мш протеин S згЩ0 Ингибитор АРС |
Тканевый фактор (ТФ)
Список обозначений:
АРС - активированный протеин С
ВМК - высокомолекулярный кининоген
ф/липиды - фосфолипиды (фрагменты клеточных мембран
TFPI - ингибитор внешнего пути свертывания
t-PA - тканевый активатор плазминогена
PAI - ингибитор активатора плазминогена
ПДФ - продукты деградации фибрина
| t-PA Урокиназа' XI 1а АРС |
JT
ПДФ (фрагмент D)
VII - фактор неактивный; Vila - активный фактор
- комплексы факторов на фосфолипидных мембранах
- ингибиторы свертывания и фибринолиза
- - активация или трансформация
- - вспомогательная активация ■ - ингибирование
Рис. 124. Схема свертывания крови (no 3.C. Баркаган, АЛ. Момот, 1998)
и образование коагуляционных (красных) тромбов.
Повреждение эндотелия является также важным фактором развития и прогрессирования атеросклероза, утолщения сосудистой стенки и возникновения облитерирующих заболеваний артерий. Дефекты же субэндотелия и его обеднение коллагеном лежат в основе ряда наследственных мезенхимальных дисплазий, протекающих с кровоточивостью и развитием аневризм сосудов и их шунтов (телеангиэктазия, или болезнь Рен-дю - Ослера, аневризмы аорты при синдроме Марфана и др.).
13.5.2. Тромбоциты и их участие в гемостазе
Тромбоциты играют главную роль в поддержании нормальной жизнедеятельности и функции эндотелиальных клеток, прочности и полноценности стенок микрососудов и в осуществлении первичного гемостаза при повреждении этих сосудов.
Образуясь из цитоплазмы полиплоидных клеток костного мозга - мегакариоцитов, тромбоциты поступают в кровь, в которой у человека их количество колеблется в пределах (150-350) • • 109/л, а продолжительность жизни составляет 8-11 дней.
Часть III. ПАТОФИЗИОЛОГИЯ ОРГАНОВ И СИСТЕМ
| ТРОМБОЦИТЫ |
| СТЕНКА СОСУДА |
| Фосфолипиды |
| Фосфолипиды |
| I |
| ■ Фосфоли- ш паза А? Арахидоновая Арахидоновая кислота кислота |
| I |
| Циклоок-сигвназа |
| PGCa,PGH2 |
| !• |
| Тромбоксан- | ^шшПроста- |
| синтентаза |
циклин-синтвтаза PGI2 (простациклин)
АГРЕГАЦИЯ
Тромбоксан Вг 6-кето-РС2„
—►переход вещества; яш^ активация; --► ингибирование
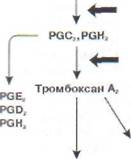
Рис. 125. Влияние простагландинов на агрегацию тромбоцитов
Основные функции тромбоцитов состоят в следующем. Они поглощаются эндотелиальны-ми клетками и поддерживают нормальную жизнедеятельность и функцию последних, способствуют их репарации. Эта функция тромбоцитов обозначается как ангиотрофическая.
При значительном уменьшении количества тромбоцитов в крови менее (20-30) • 109/л, т. е. при тромбоцитопениях, а также при ряде качественных дефектов этих клеточных элементов (тромбоцитопатиях) эндотелий становится неполноценным, вакуолизируется, легко слущива-ется, микрососуды становятся более ломкими и дольше кровоточат при повреждениях. В силу этого у больных с малым количеством или значительной дисфункцией тромбоцитов легко возникают петехиально-синячковая кровоточивость, меноррагии, носовые кровотечения, становятся положительными пробы на ломкость микрососудов - манжеточная (проба М. П. Кончаловско-го - Ремпель - Лееде), ангиорезистометрия и др., наблюдаются петехии в местах трения одеждой или мочалкой и т. п. Одновременно нарушается адгезивно-агрегационная функция тромбоцитов, в силу чего удлиняется и усиливается кровоточивость из поврежденных микрососудов. Это определяется по времени и объему кровотече-
ния из прокола кожи у края мочки уха (проба Дьюка) или из прокола кожи на ладонной поверхности верхней трети предплечья (проба Айви), после наложения на плечо манжеты для измерения АД (+40 мм рт. ст). Нормальное время кровотечения в пробе Дьюка - до 3 мин, в пробе Айви - до 6 мин. При тромбоцитопениях, тяжелых тромбоцитопатиях и при дефиците фактора Виллебранда время кровотечения резко удлиняется. Связана эта кровоточивость с недостаточностью адгезивно-агрегационной функции тромбоцитов - нарушением образования в поврежденных сосудах тромбоцитарной пробки. Это может быть обусловлено либо значительным снижением количества тромбоцитов в крови, либо их дисфунк-цией, в основе которой чаще всего лежит отсутствие или блокада на мембране тромбоцитов рецепторов, взаимодействующих со стимуляторами (агонистами) агрегации этих клеток - фактором Виллебранда (рецепторы 1в), адреналином, АДФ, фибриногеном, арахидоновой кислотой и простагландинами (рецепторы Пв/Ша), либо отсутствие в тромбоцитах или нарушение выхода из них (т. е. реакции освобождения, см. рис. 123) компонентов гранул, содержащих эти стимуляторы агрегации.
Нарушение агрегации тромбоцитов может быть связано и с рядом лекарственных воздействий, одни из которых (аспирин и др.) блокируют образование в тромбоцитах мощных циклических простагландиновых стимуляторов агрегации, в частности тромбоксана А2, другие блокируют рецепторы Пв/Ша (тиенопиридины и др.), третьи нарушают транспорт в тромбоциты ионов кальция либо стимулируют образование циклического аденозинмонофосфата (цАМФ).
Тромбоцитопатии, лежащие в основе большого числа геморрагических диатезов, подразделяют на следующие группы:
- дизагрегационные тромбоцитопатии, обусловленные отсутствием или блокадой мембранных рецепторов этих клеток (тромбастения Гланц -мана и др.);
- болезни отсутствия плотных и альфа-гранул;
- нарушения высвобождения гранул;
- нарушения образования циклических простагландинов и тромбоксана А2;
- дефицит, аномалии и нарушения мульти-мерности фактора Виллебранда;
- нарушения обмена нуклеотидов и транспорта кальция.
Исследование различных видов агрегации
Глава 13 / ПАТОФИЗИОЛОГИЯ СИСТЕМЫ КРОВИ

 тромбоцитов (агрегатометрия), изучение их ультраструктуры (определение наличия плотных и альфа-гранул), определение структуры и функции основных рецепторов этих клеток и фактора Биллебранда позволяют уточнить природу тромбоцитопатии и причину кровоточивости у обследуемого больного.
тромбоцитов (агрегатометрия), изучение их ультраструктуры (определение наличия плотных и альфа-гранул), определение структуры и функции основных рецепторов этих клеток и фактора Биллебранда позволяют уточнить природу тромбоцитопатии и причину кровоточивости у обследуемого больного.
С другой стороны, повышенная адгезивность и агрегация тромбоцитов (так называемый синдром вязких, или липких, тромбоцитов), повышение содержания и мультимерности фактора Биллебранда, как и повышение общего количества тромбоцитов в крови (тромбоцитозы), способствуют возникновению у больных тромбозов, ишемий и инфарктов органов, облитерирующих заболеваний артерий конечностей (см. разд. «Тромбофи-лические состояния»).
13.5.3. Коагуляционный гемостаз
Процесс свертывания крови - многоступенчатая ферментная реакция, в которой принимает участие ряд белков, обозначаемых как факторы свертывания крови (табл. 62). Одни из этих белков являются протеазами (факторы II, VII, IX, Х,Х1, XII, XIII), другие - акцелераторами (ускорителями) ферментных реакций (факторы V и VIII), третьи - конечным субстратом процесса (фактор I, или фибриноген). Взаимодействие факторов свертывания крови, их активация, а затем и инактивация почти на всем протяжении процесса происходят на плазменных фосфоли-пидных мембранах, от количества которых в плазме зависит либо ускорение, либо существенное замедление процесса свертывания.
Синтез ряда наиболее важных факторов свертывания (факторов V, VII, X, IX и И), а также двух основных физиологических антикоагулянтов - протеинов С и S - осуществляется паренхиматозными клетками печени - гепатоцитами, причем для того, чтобы они могли участвовать в процессе свертывания крови, все эти факторы, кроме фактора V, должны подвергнуться у-кар-боксилированию витамин К-зависимой карбок-силазой. Поэтому при дефиците витамина К и нарушении его всасывания из кишечника (при кишечном дисбактериозе, обтурации общего желчного протока), а также под влиянием непрямых антикоагулянтов (кумаринов, фенили-на), являющихся функциональными антагонистами витамина К, нарушается синтез всех витамин К-зависимых факторов свертывания, а также протеинов С и S, вследствие чего может
возникнуть тяжелая кровоточивость, сочетающаяся в некоторых случаях с микротромбировани-ем сосудов и некрозами тканей из-за недостатка антикоагулянта - протеина С.
Такое же нарушение свертываемости крови наблюдается и при тяжелых заболеваниях печени, но при этом снижается уровень в крови не только всех витамин К-зависимых факторов свертывания, но и фактора V, а также альбумина.
Различают три этапа процесса свертывания крови (см. схему на рис. 124). Первый этапзавершается активацией фактора X в так называемом протромбиназном комплексе, в состав которого входят, наряду с фактором X, фактор V, ионы кальция и фосфолипидные матрицы. Активация факторов в этом комплексе может осуществляться двумя путями: внешним и внутренним. Запуск внешнего реализуется поступлением из тканей в кровь тканевого тромбопластина (или тканевого фактора - ТФ). Свертывание по этому механизму, который в пробирке имитируется добавлением к плазме тканевого тромбопластина, обозначается как протромбиновый (тромбопластиновый) тест. Коагуляция в нем происходит очень быстро, в течение 12-15 с. При большинстве видов патологии, протекающих с развитием тромбозов или диссеминированного внутрисосудистого свертывания крови, именно этот внешний механизм свертывания крови является доминирующим.
Другим механизмом запуска процесса свертывания крови является внутренний путь. Он связан с контактом крови с субэндотелием (коллагеном), а также с разрушенными эритроцитами (при внутрисосудистом гемолизе), а в пробирке - с контактом со стеклом. При этом механизме последовательно активируются в комплексах «фактор XII (фактор Хагемана) + прекал-ликреин + фактор XI», а затем «фактор XI + + фактор IX + фактор VIII», после чего процесс, как и в предыдущем механизме, замыкается на активации фактора X с образованием протром-биназного комплекса. Внутренний механизм первого этапа свертывания протекает намного медленнее, чем внешний. Он определяется общим временем свертывания крови, временем рекальцификации цитратной плазмы и активированным парциальным тромбопластиновый временем (АПТВ).
В отличие от пробирочных опытов в организме оба указанных выше механизма свертывания крови не строго изолированы друг от друга, а
Часть III. ПАТОФИЗИОЛОГИЯ ОРГАНОВ И СИСТЕМ
Таблица 62 Факторы свертывания крови
| Цифровое обозначение | Наиболее принятые наименования | Содержание в плазме | Период полужизни в плазме после внутривенного введения | Минимальный уровень, необходимый для гемостаза | |
| г/л | % активности | ||||
| II V VII VIILC IX X XI XII XIII | Фибриноген Протромбин Тканевой тромбопластин Ас-глобулин, проакцелерин Проконвертин Антигемофильный глобулин (АГГ) РТС-фактор, фактор Кристмаса Фактор Стюарта-Прауэра РТА-фактор Фактор Хагемана, контактный фактор* Фибринстабилизирующий фактор, плазменная трансглутаминаза Плазменный прекалликреин* Высокомолекулярный кининоген (ВМК)* | 1,8-4,0 около 0,1 Около 0,01 Около 0,005 0,01-0,02 Около 0,003 Около 0,01 Около 0,005 Около 0,03 0,01-0,02 Около 0,05 Около 0,06 | 80-120 0 70-150 80-120 60-250 70-130 80-120 70-130 70-150 70-130 60-150 80-130 | 4-5 дней 2-4 дня 7 дней 23-34 ч 2-4 ч 12-18ч 20-30 ч 48-56 ч 60 ч 50-70 ч Около 4-5 дней 7 дней 7 дней | 0,8 г/л 30% 10-15% 5-10% 20-35% 20-30% 10-20% ? 3-5% |
Примечание. * - кровоточивость не возникает даже при очень глубоком дефиците (менее 1%), но существенно нарушается фибринолиз.

|
| Фибриноген |
| ТРОМБИН |
| 2 фибрино-пептида А |
| Фибрин, олигомер, -<( или РФМК |
взаимодействуют между собой. Так, имеется взаимная активация фактора Vila и комплекса «XII + калликреин», а также факторов Vila и 1Ха (см. рис. 124). Первые порции фактора Ха также ретроградно усиливают активацию комплекса «фактор VIIa+ТФ».
Второй этап свертывания крови заключается в активации протромбиназным комплексом (т. е. фактором Ха в комплексе с фактором Va + + Са2* + фосфолипидная матрица) протромбина, который, расщепляясь, превращается в активный тромбин (фактор На). Таким образом, второй этап процесса свертывания завершается образованием активного тромбина.
На третьем этапе процесса этот активный тромбин отщепляет от а- и Р-цепей фибриногена два пептида А и два пептида В, в результате чего в плазме крови повышается содержание этих пептидов и одновременно - мономеров фибрина (МФ) с четырьмя свободными связями (см. рис. 124). Вслед за этим начинается процесс полимеризации МФ - образование их димеров, затем тетрамеров и в конечном счете - волокон и сгустков фибрина (рис. 126). В связи с этим при на-
Глава 13 / ПАТОФИЗИОЛОГИЯ СИСТЕМЫ КРОВИ
28 Закш N° 532
Фибрин-полимер, или сгусток фибрина
Рис. 126. Схема трансформации фибриногена в фибрин и механизма образования РФМК
линии в крови активного тромбина в плазме повышается содержание фибринопептидов А и В, мономеров фибрина и их комплексов, обозначаемых как растворенные фибрин-мономерные комплексы (РФМК). Повышенное содержание в плазме крови всех этих промежуточных продуктов превращения фибриногена в фибрин служит показателем активации системы свертывания крови и наличия тромбинемии. Следует помнить, что тромбин является мощным стимулятором агрегации тромбоцитов и активирует фактор XIII (фибринстабилизирующий фактор), в результате чего образующиеся сгустки фибрина становятся более прочными и устойчивыми к различным растворителям (5 М мочевине, монохлоруксусной кислоте и др.).
13.5.4. Противосвертывающие механизмы и система фибринолиза
В свертывающей системе крови действуют силы как аутокатализа, или самоускорения, так и самоторможения, в силу чего многие факторы свертывания крови и их фрагменты приобретают свойства антикоагулянтов. В частности, сам фибрин и продукты расщепления фибриногена плазмином (см. ниже) обладают противосверты-вающим действием.
Однако наиболее важны для поддержания крови в жидком состоянии так называемые пер-
вичные,т. е. самостоятельно синтезируемые и постоянно находящиеся в крови, антикоагулянты(табл. 63).
Помимо перечисленных в табл. 63 важнейших физиологических антикоагулянтов, в патологических условиях в крови могут появляться в высоком титре иммунные ингибиторы факторов свертывания крови - антитела к факторам VIII, IX и другим, а также к фосфолипидным матрицам, на которых взаимодействуют и активируются факторы свертывания крови (антифос-фолипидный синдром).
Фибринолитическая (плазминовая) система,как и система свертывания крови, активируется как по внешнему, так и по внутреннему механизму (рис. 127). Наиболее мощным внешним активатором этой системы является продуцируемый в эндотелии, а также в ряде тканей тканевый плазминогеновый активатор (ТПА), на долю которого приходится около 70% всего актива-торного эффекта. Еще около 15% внешнего механизма активации приходится на фермент уро-киназу, который вырабатывается в почках и в наибольшей своей части выделяется с мочой, а в кровь попадает в значительно меньшем количестве. На остальные активаторы, поступающие в кровь извне, приходится лишь небольшая часть указанной активности, но в патологических условиях она может быть резко усилена тканевыми и лейкоцитарными протеазами, бак-
Внутрвнний механизм
Внешний механизм Активаторы
 |  | ||||||
 |  |
| Эндотели альные (ТПА) |
 Фактор XII зависимый
Фактор XII зависимый
XII>Xlla->Xllf
Прекалликреин
+ ВМ кининоген
Фактор XII независимый
Протеины C+S
Калликреин
+
ВМ кининоген
Проактиватор Активатор ПЛАЗМИ ИОГЕН
Из клеток крови
Тканевые (УК)







 Ингибитор трансформации
Ингибитор трансформации
Антиплазмины I ряда (а:-антиплазмин и др.
^ Ингибиторы II ряда
П Л А 3 М И Н
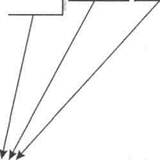
Рис. 127. Механизм активации системы фибринолиза
Часть III. ПАТОФИЗИОЛОГИЯ ОРГАНОВ И СИСТЕМ
Основные первичные антикоагулянты
Таблица 63

| Наименование | Механизмы действия |
| Ингибитор внешнего пути свертывания крови (TFPI) Тромбомодулин «Контактные ингибиторы» (фосфолипидный, плацентарный) Антитромбин III (AT III) Гепарин и другие кислые мукополисахариды Протеин С Протеин S а2-макроглобулин | Синтезируемый в эндотелии белок, инактивирующий комплекс «ТФ+фактор Vila+фактор Ха» Гликопротеин мембраны эндотелиальной клетки, связывающий и инактивирующий тромбин, в комплексе с которым тромбин сохраняет способность активировать протеин С Подавляют пусковой механизм внутреннего пути свертывания крови (комплекс факторов Х11а-Х1а и калликреина) Прогрессивно действующий ингибитор тромбина, фактора Ха и в меньшей степени других протеаз, участвующих в свертывании крови В комплексе с AT III действуют как мощные антикоагулянты Синтезируемый гепатоцитами витамин К-зависимый ингибитор факторов Villa и Va, эндогенный активатор плазминогена. Активируется тромбином и комплексом «тромбин+тромбомодулин» Синтезируемый гепатоцитами витамин К-зависимый кофактор протеина С; активируется так же, как и протеин С Слабый ингибитор комплекса «ТФ+фактор Vila», тромбина, плазмина и калликреина |
териальными активаторами (стрептокиназой, ста-филокиназой и др.) и другими экзогенными про-теолитическими ферментами (протеазами змеиных ядов и др.).
Внутренний механизм активации фибриноли-за осуществляется в основном комплексом «фактор ХПа+калликреин+высокомолекулярный кининоген» (так называемый ХПа-калликреин-
зависимый фибринолиз), активированными протеинами C+S.
Механизмы активации фибринолиза замыкаются на плазминогене, который трансформируется в активный фермент - плазмин (в прошлом он обозначался как фибринолизин).
Плазминоген и его активаторы фиксируются в основном на сгустках фибрина в тромбах, в
Фибриноген
С
300 000
J
Фрагмент X 240 000 1 + фрагменты А,В,С
Фрагменту I 155 000 83 000
Фрагмент D

|
ФрагментD
83 000
50 000
Фрагмент Е
 |  |  |
Протофибрилла


 Плазмин
Плазмин
Плазмин
DD/E
©
-®~®&У- ■(•)—(SJffi)-®- Деградационные
YD/DY ,-^7-Г YY/DXD ^ >0><v комплексы
Рис. 128. Схема расщепления
плазмином фибриногена (А) и
фибрина (Б)
Глава 13 / ПАТОФИЗИОЛОГИЯ СИСТЕМЫ КРОВИ
 связи с чем лизис фибрина преобладает над лизисом растворенного в плазме фибриногена. Кроме того, действию плазмина на фибриноген препятствует содержащийся в плазме мощный ингибитор этого фермента - а2-антиплазмин. Однако при чрезвычайно сильной активации плаз-миногена происходит истощение а2-антиплазми-на, и в плазме крови обнаруживается большое количество продуктов как фибринолиза, так и фибриногенолиза. Как видно из схем на рис. 128, эти продукты не идентичны друг другу. В результате расщепления фибриногена в плазме нарастает количество конечного продукта этого процесса - фрагмента D, тогда как при расщеплении фибрина увеличивается концентрация фрагментов D-D (димера) и D-E-D.
связи с чем лизис фибрина преобладает над лизисом растворенного в плазме фибриногена. Кроме того, действию плазмина на фибриноген препятствует содержащийся в плазме мощный ингибитор этого фермента - а2-антиплазмин. Однако при чрезвычайно сильной активации плаз-миногена происходит истощение а2-антиплазми-на, и в плазме крови обнаруживается большое количество продуктов как фибринолиза, так и фибриногенолиза. Как видно из схем на рис. 128, эти продукты не идентичны друг другу. В результате расщепления фибриногена в плазме нарастает количество конечного продукта этого процесса - фрагмента D, тогда как при расщеплении фибрина увеличивается концентрация фрагментов D-D (димера) и D-E-D.
Путем раздельного определения концентрации в плазме фрагментов D и D-димеров можно получить представление, в какой степени у больного активированы фибринолиз и фибриногено-лиз. Более того, при проведении таких анализов учитывается, что для нарастания в крови продуктов фибринолиза, т. е. D-димера, должно раньше произойти свертывание крови - образование фибрина, а затем его расщепление до фрагмента D-D. Поэтому увеличение концентрации в плазме D-димера служит ценным показателем как интенсивного внутрисосудистого свертывания крови, так и сопряженного с этим процессом фибринолиза. Такое нарастание содержания в крови D-димера является важным маркером массивного тромбоза кровеносных сосудов, тромбоэмболии, диссеминированного внутрисосудистого свертывания крови.
13.5.5. Геморрагические диатезы и синдромы
К геморрагическим диатезам и синдромам относят все те виды патологии, для которых характерна наклонность к кровоточивости системного характера. Эти виды патологии подразделяют на наследственные (врожденные) и приобретенные формы. Среди последних преобладают вторичные и симптоматические нарушения гемостаза.
В зависимости от того, нарушения в каком звене системы гемостаза стали причиной кровоточивости, все заболевания этой группы подразделяют на следующие: