Функции тромбоцитов.
Кровяные пластинки образуют главную линию обороны организма против внезапных потерь крови. Они аккумулируются почти тотчас вместе повреждения кровеносных сосудов и закупоривают их вначале временной, а затем постоянной тромбоцитарной пробкой, облегчают превращение фибриногена в фибрин в поврежденном участке.
Структура и функции тромбоцитов.Циркулирующие в крови тромбоциты имеют дисковидную форму, диаметром от 2 до 5 мкм, объемом 5- 10 мкм3. Тромбоциты оказались весьма сложным клеточным комплексом, представленным системами мембран, микротрубочек, микрофиламентом и органелл. Используя технику, позволяющую разрезать распластанный тромбоцит параллельно поверхности, в клетке выделяют несколько зон: периферическую, золя-гель, внутриклеточных органелл (рис.6.4.). На наружной поверхности периферической зоны располагается покров, толщиной до 50 нм, содержа-
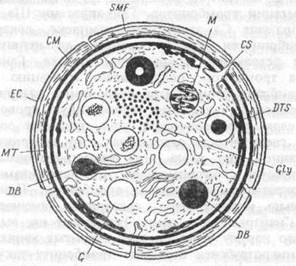
Рис.6.4. Ультраструктурная организация тромбоцита.
Сечение параллельное горизонтальной плоскости.
ЕС — периферическая зона тромбоцита, СМ — трехслойная мембрана, SMF — субмембранный филомент, МТ— микротрубочки, Gly — гликоген. Зона органнелл — М — митохондрии, G — гранулы, DB — плотные гранулы, DTS — система плотных трубочек, CS — система открытых канальцев.
21У
щий плазматические факторы свертывания крови, энзимы, рецепторы, необходимые для активации тромбоцитов, их адгезии (приклеивания к субэндотелию) и агрегации (приклеиванию друг к другу). Так, мембрана тромбоцитов содержит "мембранный фосфолипидный фактор 3" — "фосфолипидную матрицу", формирующую активные коагуляционные комплексы с плазменными факторами свертывания крови. Мембрана богата также арахидоновой кислотой, поэтому важным ее компонентом является фермент — фосфолипаза А,, способная образовывать свободную арахидоновую кислоту для синтеза простагландинов, из метаболитов которых формируется короткожи-вущий агент — тромбоксан А2, вызывающий мощную агрегацию тромбоцитов. Активация фосфолипазы А2 в мембране тромбоцита осуществляется при ее контакте с коллагеном и фактором Вилле-бранда — адгезивными белками субэндотелия, обнажающимися при повреждении эндотелия сосудов.
В липидный бислой мембраны тромбоцитов встроены гликопро-теины I, II, III, IV, V. Гликопротеин I состоит из субединиц — Iа, Iв, Iс. Iа — рецептор, ответственный за адгезию тромбоцитов к коллагену субэндотелия. Комплекс "Iв — фактор свертывания крови IX" на поверхности кровяных пластинок выполняет функцию рецептора для фактора Виллебранда, что также необходимо для адгезии пластинок на субэндотелии. Iс обеспечивает связывание с еще одним адгезивным белком субэндотелия — фибронектином, а также распластывание пластинки на субэндотелии.
Гликопротеин II состоит из субединиц IIа и IIв, необходимых для всех видов агрегации тромбоцитов. Гликопротеин Ша с гликопро-теином IIв образуют Са-зависимый комплекс, связывающий на тромбоцитах фибриноген, что обеспечивает дальнейшую агрегацию тромбоцитов и ретракцию (сокращение) сгустка. Гликопротеин V гидролизируется тромбином, поддерживает агрегацию тромбоцитов. Снижение в мембране тромбоцитов содержания различных субединиц гликопротеинов I-V вызывает повышенную кровоточивость.
К нижнему слою периферической зоны прилегает зона золя-геля гиалоплазмы, в свою очередь отделяющая зону внутриклеточных ор-ганелл. В указанной зоне вдоль края клетки располагается краевое кольцо микротрубочек, контактирующее с микрофиламентом, представляющим сократительный аппарат тромбоцита. При стимуляции тромбоцита кольцо микротрубочек, сокращаясь, смещает гранулы к центру клетки ("централизация гранул"), сжимает их, вызывая секрецию содержимого наружу через систему открытых канальцев. Сокращение кольца микротрубочек позволяет тромбоциту также образовывать псевдоподии, что увеличивает его способность к агрегации.
Зона органелл тромбоцитов содержит плотные гранулы, альфагра-нулы 1 и II типов. В плотных гранулах находятся АДФ, АТФ, кальций, серотонин, норадреналин и адреналин. Кальций участвует в регуляции адгезии, сокращении, секреции тромбоцита, активации его фосфолипаз и, следовательно, продукции эндоперекиси, простагландинов, в ходе дальнейших превращений которых образуется тромбоксан А,. АДФ секретируется в больших количествах при ад-
220
гезии тромбоцитов к стенке сосуда и способствует прикреплению циркулирующих тромбоцитов к адгезированным, тем самым поддерживая рост тромбоцитарного агрегата. Серотонин (5-гидроксит-риптамин) секретируется тромбоцитом во время "реакции освобождения гранул" и обеспечивает вазоконстрикцию в месте повреждения.
Альфа-гранулы I типа содержат антигепариновый фактор пластинок 4, фактор роста тромбоцитов, тромбоспондин (гликопротеин G) и др. Антигепариновый фактор тромбоцитов 4 секретируется тромбоцитами под влиянием АДФ, тромбина, адреналина, сопровождая агрегацию тромбоцитов. Тромбоспондин образует комплекс с фибриногеном на поверхности активированных тромбоцитов, необходимый для формирования тромбоцитарных агрегатов. Тромбоцитарный ростковый фактор (ТРФ) — полипептид, стимулирующий рост гладких мышц сосудов и фибробластов, восстановление сосудистой стенки и соединительной ткани. Благодаря его свойствам, кровяные пластинки поддерживают целостность сосудистой стенки. Больные с тромбоцитопенией имеют сниженную устойчивость стенки капилляра, поэтому петехии (точечные кровоизлияния в коже) появляются вслед за легкими травмами или изменением давления крови. Петехии вызваны слущиванием эндотелия капилляров. В нормальных условиях возникший дефект устраняется пластинками, секретиру-ющими ТРФ.
Альфа- гранулы II типа содержат лизосомальные энзимы (кислые гидролазы). Большая часть гранул исчезает после адгезии или агрегации тромбоцита. Этот феномен ("реакция освобождения гранул") имеет место после активации тромбоцита различными соединениями — тром-боксаном А2, АДФ, адреналином, тромбином, протеолитическими энзимами, бактериальными эндотоксинами, коллагеном и др.
Тромбоцитопоэз и его регуляция.Под тромбоцитопоэзом понимают процесс образования тромбоцитов в организме. В основном, он протекает в костном мозге и включает следующие этапы: коло-ниеобразующая единица мегакариоцитарная (КОЕ-мег) -> промега-кариобласт -> мегакариобласт -> промегакариоцит -> зрелый мегака-риоцит -> тромбоцитогенный мегакариоцит -> тромбоциты (рис.6.5.).
Истинные митозы, т.е. деление клеток, присущи только КОЕ-мег. Для промегакариобластов и мегакариобластов характерен эндомитоз (глава I), т.е. удвоение ДНК в клетке без ее деления. После остановки эндомитоза, в основном после 8, 16, 32, 64-кратного удвоения ДНК, мегакариобласт начинает дифференциацию до тромбоцитарного мегакариоцита, образующего тромбоциты.
В костном мозге тромбоцитогенные мегакариоциты локализованы преимущественно на поверхности синусного эндотелия и их цито-плазматические отростки проникают в просвет синуса через эндотелий. Одни из них проникают на 1-2 мкм в просвет синуса и фиксируют мегариоцит на эндотелии (функция "якоря"). Второй тип отростков представлен вытянутыми цитоплазматическими лентами (до 120 мкм в длину), входящими в просвет синуса и получившими
221

Рис.6.5. Схема дифференцировки клеток мегакариоцитарной серии.
СКК — стволовая кроветворная клетка; КОЕгммэ — КОЕгрануло-цитарно-мегакариоцитарно-моноцитарно-эритроцитарная; КОЕэрмег — КОЕэритроцитарно-мегакариоцитарная; КОЕмег — КОЕмегакариоцитарная; КОЕмег-1 — менее дифференцированная; КОЕмег-2 — более дифференцированная клетка; 0.07, 0.48, 0.74 — вероятность вовлечения клетки-предшественницы в мегакариоцитарную дифференциацию.
название протромбоцитов. Их количество у одного мегакариоцита может достигать 6-8. В просвете синуса цитоплазма протромбоцита после локальных сокращений разрывается, и он образует около 1000 тромбоцитов. В циркулирующее русло поступают и протромбоциты. Вышедшие в кровь протромбоциты достигают микроциркуляторного русла легких, где из них освобождаются тромбоциты. Поэтому количество тромбоцитов оказывается более высоким в легочных венах, чем в легочной артерии. Количество тромбоцитов, образовавшихся в легких, может достигать 7- 17% от массы тромбоцитов в крови.
У человека время полного созревания мегакариоцитов занимает 4-5 дней. Костный мозг человека содержит около 15.106 мегакари-оцитов/кг веса тела. Дневная продукция тромбоцитов у человека 66000+14600 в 1 мкл крови. В среднем мегакариоцит высвобождает до 3000 тромбоцитов. Количество тромбоцитов в крови взрослого человека достигает 150-375.109л; у детей —150-250- 109/л. Содержание тромбоцитов в крови взрослого ниже 150.10 9/л рассматривается как тромбоцитопения.
Общая популяция тромбоцитов представлена циркулирующими в крови (70%) и находящимися в селезенке (30%). Накопление тром-
222
боцитов в селезенке происходит благодаря более медленному их движению через извилистые селезеночные корды и занимает до 8 минут. Сокращение селезенки (например, вызванное адреналином) освобождает пластинки в общий кровоток. Существование селезеночного депо тромбоцитов объясняет, почему их количество неизменно выше у спленэктомированных (с удаленной селезенкой) людей, чем у нормальных индивидуумов. У пациентов со спленомега-лией (увеличенной селезенкой) значительная часть циркулирующих тромбоцитов медленно продвигается через увеличенную селезенку, количество пластинок в крови оказывается сниженным, возникает тяжелая тромбоцитопения.
Продолжительность жизни тромбоцитов человека колеблется от 6,9 до 9,9 дней. Их разрушение происходит, преимущественно, в костном мозге и, в меньшей степени, в селезенке и печени.
В плазме крови людей обнаружен колониестимулируюший фактор мегакариоцитарный (КСФ-мег), стимулирующий митозы и дифференциацию КОЕ- мег. Стимулом для его образования является истощение содержания мегакариоцитов и их предшественников в костном мозге. Регуляция тромбоцитопоэза в фазу немитотического развития мегакариоцитов осуществляется другим гуморальным фактором — тромбопоэтином. Его количество в плазме повышается при усилении потребления тромбоцитов (воспаление, необратимая агрегация тромбоцитов). Тромбопоэтин необходим для полного созревания цитоплазмы мегакариоцитов, нормального формирования в ней тромбоцитов. Регуляция мегакариоwитопоэза включает и особые вещества — его гуморальные ингибиторы, угнетающие как пролифе-ративную, так и немитотическую стадии развития мегакариоцитов. Ингибитор деления КОЕ-мег выделен из активированных тромбоцитов. Это гликопротеин, массой в 12-17 кд. Источником ингибитора тромбоцитопоэза является, также, селезенка.
6.4. Механизмы гемостаза.
Тромбоцитарный гемостаз.Тромбоцитарная реакция, т.е. реакция тромбоцитов на нарушение целостности сосудистой стенки, формируется параллельно реакции самих сосудов на повреждение — их сокращение в месте повреждения, шунтирование крови выше поврежденного участка. Поскольку сосудисто-тромбоцитарная реакция на повреждение первой обеспечивает остановку кровотечения из микрососуда, то ее называют сосудисто- тромбоцитарным или первичным гемостазом, а формирование и закрепление тромбов — вторичным коагуляционным гемостазом. Первая волна агрегации тромбоцитов связана с их адгезией к пластинкам, приклеившимся рецепторами гликопротеинов I и II к фактору Виллебранда, фибро-нектину и коллагену субэндотелия поврежденных тканей. Вторая волна агрегации вызвана высвобождением АДФ из плотных гранул тромбоцитов, образованием тромбоксана А, в их мембране, взаимодействием мембранных гликопротеинов Ив-Шс с фибриногеном, V — с тромбином.
223
Вторую волну агрегации тромбоцитов обеспечивают тромбоксан А2 и тромбин. Мощным стимулом для образования тромбоксана А2 являются коллаген и фактор Виллебранда, активирующие фосфоли-пазу A2. Тромбин, образуемый на мембране кровяной пластинки, благодаря секреции ею фактора V и взаимодействию его с глико-протеином V, начинает быстро действовать как сильный агрегаци-онный агент. Новые порции тромбоцитов соприкасаются с адгези-рованными тромбоцитами, начинается агрегация вновь принесенных кровью клеток, и вновь включаются вышеописанные механизмы, а это, в свою очередь, усиливает агрегацию новой партии тромбоцитов и т.д. Тромбоцитарный тромб уплотняется и сокращается. Его формирование усиливается образованием фибрина (фибринового тромба) вследствие активации системы свертывания крови.
Система свертывания крови.Эта система обеспечивает остановку кровотечения, благодаря образованию фибриновых тромбов. В физиологических условиях большинство факторов свертывания крови содержится в ней в неактивном состоянии, в виде неактивных форм ферментов, обозначаемых римскими цифрами: I, II, VIII, IX, X, XI, XII, XIII(табл.6.3.). Однако повреждение сосуда или клеток крови приводит к активации этих ферментов. При этом переход в активное состояние одного фактора вызывает активацию следующего, образуя каскадную реакцию, заканчивающуюся образованием фибриновых нитей, формирующих сеть тромба (рис.6.6.). В начале этой реакции в крови, в зоне поврежденного сосуда образуется активная протромбо-
Таблица6.3 Факторы свертывания крови
| Фактор | Период | Молекулярная | Нормальная | |
| полужизни | масса | концентрация | ||
| (дальтон) | в плазме | |||
| (мг/мл) | ||||
| 1 _ | фибриноген | 3,7 дня | 340.000 | 1500-4000 |
| II - | - протромбин | 2,8 дня | 72.500 | |
| III - | - тромбопластин | — | — | |
| IV ■ | - ионы кальция | — | — | 0,9-1,2 ммоль/л |
| V - | - проакцелерин | 15-24 ч | 330.000 | |
| VI - | - проконвертин | 1,2-6 ч | 48.000 | менее 1 |
| VII | с — антигемофилический А | 5-12 ч 1 | менее 0,5 | |
| VIII | ФВ — фактор Виллебранда | 24-40 ч 1 | I .UUU.UUU | |
| IX - | - антигемофильный фактор Б, | 20-24 ч | 57.000 | |
| фактор Кристнаса | ||||
| X - | - фактор Стюарта-Прауэра | 32-48 ч | 59.000 | |
| XI - | - антигемофильный фактор В, | 40-48 ч | 160.000 | |
| предшественник плазменного | ||||
| тромбопластина | ||||
| XII | — фактор Хагемана | 48-52 ч | 76.000 | |
| XIII | — фибрин-стабилизирующий | 5-12 дней | 320.000 | |
| фактор | ||||
| Плазминоген | 2,2 дня | 90.000 | ||
| Прекалликреин (фактор Флетчера) | — | 85.000 | ||
| Высокомолекулярный кениноген | — | 150.000 |
224
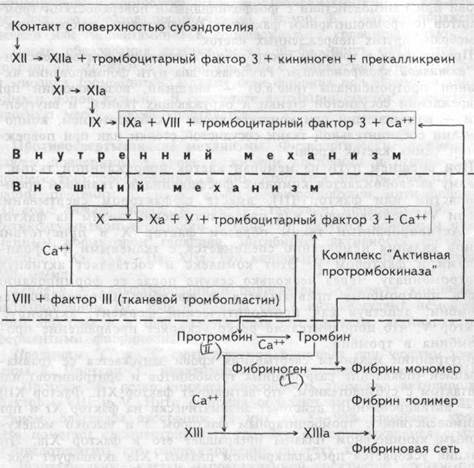
Рис.6.6. Схема последовательной активации факторов свертывания крови.
а — активированный.
киназа, превращающая неактивный протромбин в тромбин — активный протеолитический фермент, отщепляющий от молекулы фибриногена 4 пептида мономера. Каждый из мономеров имеет 4 свободных связи. Соединяясь ими друг с другом, конец к концу, бок к боку, они в течение нескольких секунд формируют волокна фибрина. Их сеть вначале слаба, однако под влиянием фибрин-стабилизирующего фактора (фактора XIII), также активируемого в крови тромбином в присутствии ионов кальция, в фибрине образуются дополнительные ди-сульфидные связи и сеть фибриновых волокон становится прочной. В этой сети задерживаются тромбоциты, лейкоциты, эритроциты и белки плазмы, формируя фибриновый тромб.
В крови содержатся и неферментные белки — акселераторы, также обозначаемые римскими цифрами (фактор V, VII), обеспечивающие ускорение во много тысяч раз течение реакции свертывания
225
крови при взаимодействии с фосфолипидными поверхностями тромбоцитов (с тромбоцитарным фактором 3), участками мембран (мик-ромебран) других поврежденных клеток.
Превращение в тромбин протромбина происходит под воздействием активной протромбиназы. Различают два пути формирования активной протромбиназы (рис.6.6) — внешний, возникающий при повреждении сосудистой стенки и окружающих тканей, и внутренний — возникающий при контакте крови с субэндотелием, компонентами соединительной ткани сосудистой стенки или при повреждении самих клеток крови.
При внешнем пути из мембран клеток поврежденной ткани в плазму высвобождается комплекс фосфолипидов (тканевой тром-бопластин или фактор III), вместе с фактором свертывания крови VII действующий как протеолититеский энзим на фактор X. Активированный таким образом фактор X в присутствии ионов кальция немедленно соединяется с тканевыми фосфоли-пидами и фактором V. Этот комплекс и составляет активную протромбиназу. Через несколько секунд после ее формирования часть протромбина превращается в тромбин. Образовавшийся тромбин, действуя как протеолитический фермент, активирует фактор V, что дополнительно резко ускоряет превращение протромбина в тромбин.
Внутренний механизм свертывания крови запускается ее травма-тизацией (появление разрушенных тромбоцитов и эритроцитов) или контактом с субэндотелием, что активирует фактор XII. Фактор ХПа (а — активированный) действует энзиматически на фактор XI и при взаимодействии с тромбоцитарным фактором 3 и высоко молекулярным кининогеном плазмы превращает его в фактор ХIа. Эта реакция ускоряется прекалликриином плазмы. ХIа активирует фактор IX (антигемофильный фактор В). После образования фактора IХа формируется комплекс: "фактор IХа + фактор VIII (антигемофильный глобулин А,) + тромбоцитарный фактор 3 + ионы кальция". Этот комплекс активирует фактор X. Фактор Ха образует с фактором V и тромбоцитарным фактором 3 новый комплекс, называемый протромбиназой, который в присутствии ионов кальция в считанные секунды превращает протромбин в тромбин.
Следует подчеркнуть весьма важную роль фосфолипидной матрицы (тромбоцитарного фактора 3) в повышении активности протромбиназы — при отсутствии фосфолипидной матрицы ее активность снижается в 1000 раз!
Нарушенное формирование комплекса, активирующего фактор X, сопровождается нарушениями гемостаза. Так, тромбоцитопения, создавая дефицит тромбоцитарного фактора 3, приводит к геморрагическому диатезу, дефицит фактора IX вызывает гемофилию В, дефицит фактора VIII — гемофилию А.
Активация протромбокиназы по внешнему пути занимает около 15 секунд, а по внутреннему — 2-10 минут. Активированная протром-бокиназа и ионы кальция превращают протромбин в тромбин. Количество образующегося тромбина прямо пропорционально количеству
226
активированной протромбокиназы. Протромбин синтезируется в печени, для его образования необходим витамин К, поэтому поражение печени или гиповитаминоз К сопровождаются кровоточивостью.
После образования сгустка через 30-60 минут начинается его сокращение {ретракция). Оно связано с сокращением нитей актина и миозина тромбоцитов, а также сети фибрина под влиянием тромбина и ионов кальция. В результате ретракции сгусток сжимается в плотную массу, тромб уплотняется.
Противосвертывающие механизмы.Физиологические антикоагулянты поддерживают кровь в жидком состоянии и ограничивают процесс тромбообразования. К ним относятся антитромбин III,гепарин, протеины "С" и "S", альфа-2-макроглобулин, нити фибрина. На долю антитромбина III (альфа-2-глобулин) приходится 75% всей антикоагулянтной активности плазмы. Он является основным плазменным кофактором гепарина, ингибирует активность тромбина, факторов Ха, IXa, VIIa, XIIa. Его концентрация в плазме достигает 240 мг/мл.
Гепарин — сульфатированный полисахарид. Образует комплекс с антитромбином III,трансформируя его в антикоагулянт немедленного действия и в 1000 раз усиливая его эффекты, активируя неферментный фибринолиз.
Протеины "С" и "S" синтезируются в печени при участии витамина К. Протеин "С" инактивирует активированные факторы VIII и V. Протеин "S" резко снижает способность тромбина активировать факторы VIIIи V. Нити фибрина обладают антитромбинным действием, благодаря адсорбции на них до 85-90% тромбина крови. Это помогает сконцентрировать тромбин в формирующемся сгустке и предотвратить его распространение по току крови.
Эндотелиальные клетки неповрежденной сосудистой стенки препятствуют адгезии тромбоцитов на ней. Этому же противодействуют гепариноподобные соединения, секретируемые тучными клетками соединительной ткани, а также простациклин, синтезируемый эндо-телиальными и гладкомышечными клетками сосуда, активация протеина "С" на эндотелии сосуда. Гепариноподобные соединения эндотелия (и гепарин крови) усиливают антикоагуляционную активность антитромбина III.Простациклин является мощным ингибитором агрегации тромбоцитов. В физиологических условиях он образуется в венозных и артериальных эндотелиальных клетках из ара-хидоновой кислоты, через этап формирования эндоперекисей про-стагландинов. В результате между образующейся в тромбоцитах про-агрегационной субстанцией — тромбоксаном А2 и антиагрегационной активностью простациклина сосудистой стенки возникает динамическое равновесие, регулирующее агрегацию тромбоцитов. Сниженная или утраченная продукция простациклина участком эндотелия может быть одной из причин агрегации кровяных пластинок и вести к формированию тромба.
Тромбомодулин — рецептор тромбина на эндотелии сосудов взаимодействуя с тромбином, активирует белок "С", обладающий
227
способностью высвобождать тканевой активатор плазминогена из стенки сосуда. Дефицит белка "С" сочетается с повышенной свертываемостью крови, наклонностью к тромбозам. Свертывание крови в сосуде предупреждает и гладкая поверхность эндотелия, препятствующая включению внутреннего пути формирования активной протромбиназы. Мономолекулярный слой белка, адсорбированный на поверхности эндотелия, отталкивает факторы свертывания и тромбоциты, также предупреждая свертывание крови.
Фибринолиз — это процесс разрушения {лизиса) сгустка крови, связанный с расщеплением фибрина, фибриногена на мелкие фрагменты. Важнейшая функция фибринолиза — восстановление просвета сосудов, закупоренных тромбами. Расщепление сгустка крови осуществляется системой ферментов, активными компонентами которой являются плазмин — протеолитический фермент, расщепляющий нити фибрина, а также фибриноген, факторы свертывания крови V, VII, XII и протромбин.
В плазме крови содержится неактивная форма фермента плазминогена — белок плазминоген. Существует несколько механизмов его активации. Одни из них связан с высвобождением белкового тканевого активатора из эндотелиальных клеток на участке формирующегося кровяного сгустка. Активировать плазминоген могут также активированный фактор свертывания крови XII при взаимодействии с калликриином и высокомолекулярным кининогеном, а также ли-зосомальные ферменты поврежденной ткани. Активатором плазминогена является урокиназа, образующаяся в почках и выделяющаяся с мочой. В кровь попадает ее небольшое количество, и с ней связано лишь около 15% общей фибринолитической активности. Активатором плазминогена является стрептокиназа бактерий. Данным действием стрептококков в инфицированных тканях объясняют растворения плазменного сгустка в лимфе и тканевой жидкости и распространение инфекции.
Активный плазмин блокируется антиплазминами. Наиболее деятельным является а2-антиплазмин (а2-глобулин), способный нейтрализовать 2/3 всего плазмина. Другой ингибитор фибринолиза — а2- макроглобулин. Продукты, образующиеся в ходе фибринолиза, тормозят агрегацию тромбоцитов и формирование волокон фибрина, тормозят фибринолиз. Лизис кровяных сгустков продолжается в течение нескольких дней. Выброс тканевых активаторов фибринолиза имеет место под влиянием физических нагрузок, адреналина, норадреналина.
6.5. Общие закономерности кроветворения.
Кроветворные клетки-предшественницы.Ежечасно у здорового человека в крови погибает 20 миллиардов тромбоцитов, 10 миллиардов эритроцитов и 5 миллиардов лейкоцитов. Эта непрерывная утрата клеток постоянно компенсируется равным ей количеством вновь образующихся форменных элементов крови. Масштаб этого восполнения огромен: примерно каждые два года в организме че-
228
ловека производится масса клеток крови, равная массе его тела. Указанный огромный пролиферативный потенциал кроветворной ткани заключен в стволовых кроветворных клетках (СКК) — предшественницах, способных к самообновлению, т.е. производству дочерних СКК на протяжении всей жизни человека. СКК диффрен-цируется: 1) в направлении клетки-предшественницы всех линий миелопоэза, т.е. гранулоцитопоэза, моноцитопоэза, мегакариоцито-поэза и эритропоэза; 2) в направлении клетки-предшественницы Т-лимфоцитов; 3) клетки-предшественницы В-лимфоцитов (рис.6.7.)-Эти клетки-предшественницы получили название колониестимули-рующих единиц (КОЕ) или колониеобразующих клеток (КОК), от формируемых ими при культивировании ин витро колоний. Так, КОЕ-ГММЭ — гранулоцитарно-макрофагально-мегакариоцитарно-эритроцитарная колониеобразующая единица получила название от формируемой ею колонии, состоящей из гранулоцитов, макрофагов, мегакариоцитов и эритроцитов; пре-КОЕ-Т — от колонии, состоящей из Т- клеточных субпопуляций; пре-КОЕ-В — от колонии, состоящей из В-лимфоцитов. КОЕ-ГММЭ в ходе дифференциации формируют би- и унипотентные КОЕ, которые также классифицируют на основании произведенного ими потомства при культивировании ин витро. Так, нейтрофильные гранулоциты и макрофаги образуются из одной общей КОЕ. Поэтому возникло ее название — КОЕ-гранулоцитарно-моноцитарная (КОЕ-ГМ). КОЕ, образующая колонии из эритроидных клеток и мегакариоцитов, называется эрит-роиитарно-мегакариоцитарной (КОЕ-Эмег) и т.п. Это примеры бипотентных клеток, т.е. клеток, дифференцирующихся в направлении каких-либо двух линий гемопоэза. Формирующиеся из них унипотентные КОЕ образуют колонии из клеток только одной линии. В связи с этим возникли их названия — КОЕ-эритроцитар-ные, эозинофильные, базофильные, нейтрофильные, мегакариоци-тарные.
Бипотентные КОЕ обладают значительной способностью к размножению. Например, КОЕ-Эмег, будучи стимулированной ростковыми факторами, способна совершать до 13 митозов и образовывать несколько десятком КОЕ-Э, из которых далее формируется несколько тысяч эритроидных клеток. Количество КОЕ-Эмег достигает 30-40 на 105 клеток костного мозга, а содержание КОЕ-Э в нем почти в 10 раз выше, чем КОЕ-Эмег. Из каждой КОЕ-Э образуется до 50 эритроцитов. КОЕ-ГМ способна совершать 5-6 делений, образующиеся из нее КОЕ-Г и КОЕ-М —еще 5-6 делений каждая. Это позволяет одной КОЕ-ГМ формировать тысячи зрелых клеток-потомков — гранулоцитов и моноцитов.
Дифференциация клеток-предшественниц КОЕ-ГММЭ до унипо-тентных КОЕ сопровождается формированием рецепторов к гемопо-этическим гормонам (интерлейкину-3, КСФ-ГМ, эритропоэтину, тромбоцитопоэтину), к нейромедиаторам, катехоламинам, тиреотроп-ному гормону, производным тестостерона, поэтому указанные гормоны регулируют пролиферацию и дифференциацию клеток крови.
229
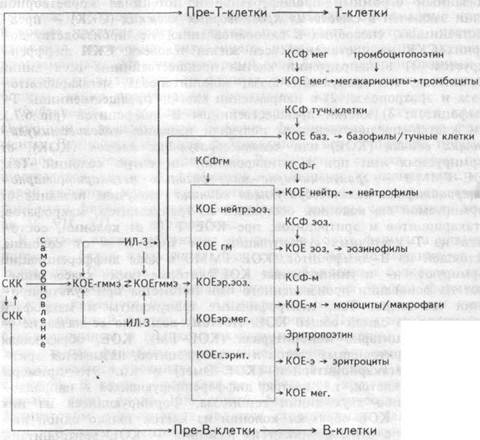
Рис.6.7. Схема развития гемопоэтических клеток и регулирующие их колониестимулирующие факторы.
СКК — стволовая кроветворная клетка;
КОЕ-ГММЭ — колониеобразующая единица гранулоцитарно-моноци-
тарно-мегакариоцитарно-эритроцитарная;
КОЕ нейтр.эоз. — КОЕ нейтрофильно-эозинофильная;
КОЕ-гм — КОЕ гранулоцитарно-моноцитарная;
КОЕ эр.эоз. — КОЕ эритроцитарно-эозинофильная;
КОЕ эр.мег. — КОЕ эритроцитарно-мегакариоцитарная;
КОЕ г.эрит. — КОЕ гранупоцитарно-эритроцитарная;
КОЕ мег. — КОЕ мегакариоцитарная;
КОЕ баз. — КОЕ базофильная; КОЕ нейтр. — КОЕ нейтрофильная;
КОЕ эоз. — КОЕ эозинофильная; КОЕ-мс — КОЕ моноцитарная;
КСФ — колониестимупирующий фактор;
КСФ-мег — КСФ мегакариоцитов; КСФ-г — КСФ гранулоцитов;
КСФ-баз. — КСФ базофилов; КСФ-м — КСФ моноцитов;
КСФ-эоз. — КСФ эозинофилов.
230
Регуляция пролиферации и дифференциации КОЕ (КОК).Рост различных КОЕ в культурах удается получить, добавляя стимулирующие его факторы. Отсюда факторы, стимулирующие образование гра-нулоцитарных колоний, получили название "колониестимулирующие факторы гранулоцитарные" — КСФ- Г, макрофагальных — КСФ- М, гранулоиитарно- макрофагальных — КСФ- ГМ, эозинофильных — КСФэоз, мегакариоиитарных — КСФмег, стимулирующие развитие колоний из КОЕ-ГММЭ — мульти-КСФ (позже обозначенные как интерлейкин 3 — ИЛ-3). Установлено, что ИЛ-3 и КСФ-ГМ стимулируют пролиферацию и дифференциацию не только КОЕ-ГММЭ и КОЕ-ГМ, но и других бипотентных КОЕ. В связи с этим, ИЛ-3 и КСФ-ГМ рассматривают как факторы неспецифические, поддерживающие самообновление и пролиферацию КОЕ-ГММЭ и бипотенциаль-ных. Все КСФ-ы гликопротеины, относимые ныне к семье полипептидных гормонов, регулирующих гемопоэз. Источниками ИЛ-3 и КСФэоз являются Т-лимфоциты, спленоциты; КСФ-ГМ — Т-лимфоциты, моноциты, эндотелиальные клетки и фибробласты; КСФ- Г, КСФ- М — моноциты и фибробласты; эритропоэтина — перитубуляр-ные клетки почек, купферовские клетки печени.
Гены, контролирующие синтез ИЛ-3, КСФ-Г и КСФ-М у человека, находятся на дистальной части длинного плеча 5 хромосомы, КСФ-Г — локализованы у человека на 17 хромосоме, эритропоэтина — на 7 хромосоме. Нарушение участков генома, ответственных за синтез молекулярных регуляторов гемопоэза, вызывает у человека тяжелые нарушения в системе крови. Продукцию КСФ усиливают различные стимулы: гипоксия —эритропоэтина, тромбо-цитопения — тромбоцитопоэтина, микробная инфекция — КСФ-ГМ, КСФ-Г, КСФ-М, гельминтная инфекция — КСФэоз. Но каждый из перечисленных раздражителей одновременно стимулирует в организме и продукцию неспецифических ростковых факторов — ИЛ-3, КСФ-ГМ и других. При этом ИЛ-3 и КСФ-ГМ стимулируют как пролиферацию КОЕ-ГММ и КОЕ бипотентных, так и формирование на их мембране рецепторов к КСФ-ам, действие которых направлено на унипотентные КОЕ. Высокие же концентрации КСФ- Г, КСФ- М и других стимулируют пролиферацию и дальнейшую дифференциацию унипотентных клеток-предшественниц гранулоцитарного, моноцитарного и др. рядов.
На интенсивность продукции КСФ-ов оказывает регулирующее влияние вегетативная нервная система. Так, введение животным а-и В-адреноблокаторов значительно уменьшает уровень КСФ-ов в крови. Стимулируют гемопоэз Т-лимфоииты. Так, действие на организм возбуждающих гемопоэз факторов (кровопотеря, высотная гипоксия и др.) вызывает миграцию лимфоцитов в костный мозг и активацию ими КОЕ. КСФ-ы регулируют функции не только КОЕ, но и зрелых клеток крови. Так, КСФ- м усиливает фагоцитарную активность, метаболизм, миграцию в ткани зрелых нейтрофилов и моноцитов-макрофагов. КСФ-Г стимулирует бактерицидную, фагоцитарную и цитотоксическую активность этих клеток. ИЛ-3 также усиливает цитотоксическую активность макрофагов, увеличивает
231
эозинофильную фагоцитарную активность, а КСФ- М — бактерицидную и тумороцидную (разрушающую опухолевые клетки) функции моноцитов и макрофагов.