Краткая теория
Заметное отклонение молекул от прямолинейных траекторий при тепловом движении происходит только при их достаточном сближении. Такое взаимодействие между молекулами называется столкновением. Процесс столкновения молекул удобно характеризовать величиной эффективного диаметра молекулы. Под ним понимается минимальное расстояние, на которое могут сблизиться центры двух молекул при их столкновении.
Расстояние, которое проходит молекула между двумя последовательными соударениями, называется средней длиной свободного пробега.
Молекулярно-кинетическая теория позволила получить формулы, связывающие макроскопические параметры газа (давление, объем, температуру) с его микроскопическими параметрами (размеры и масса молекулы, её скорость, средняя длина свободного пробега). Пользуясь этими формулами, можно на основании измеренных макропараметров газа найти его микроскопические параметры.
Коэффициент внутреннего трения газа h связан со средней длиной свободного пробега álñ, средней арифметической скоростью молекул áuñ и плотностью газа r формулой
 . (6)
. (6)
Из формулы (6) получаем
 . (7)
. (7)
Вязкость h можно определить, воспользовавшись известной формулой Пуазейля, выражающей вязкость через объем газа V, протекающего через сечение трубки (капилляра) за время t при определенной разности давлений Dр на концах капилляра:
 , (8)
, (8)
где r – радиус капилляра; l – длина капилляра.
Средняя скорость молекул газа может быть найдена из распределения Максвелла:
 , (9)
, (9)
где R – газовая постоянная; Т – термодинамическая температура; М – молярная масса газа.
Плотность газа можно найти из уравнения Менделеева-Клапейрона:
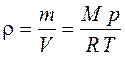 , (10)
, (10)
где p – давление газа.
Подставляя формулы (9) и (10) в формулу (7), получим:
 . (11)
. (11)
Эффективный диаметр молекулы можно вычислить из формулы, выражающей его связь с длиной свободного пробега:
 , (12)
, (12)
где n – концентрация молекул при данных условиях; d – эффективный диаметр молекулы.
Концентрация молекул при данных условиях (p, T) выражается формулой:
 , (13)
, (13)
где n0 – (число Лошмидта) число молекул в единице объема при нормальных условиях (p0, T0).
Используя формулы (12) и (13), получаем выражение для эффективного диаметра молекулы газа:
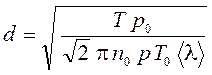 . (14)
. (14)