ОПРЕДЕЛЕНИЕ ПОКАЗАТЕЛЯ ПУАССОНА ВОЗДУХА
КРАТКАЯ ТЕОРИЯ. Теплоемкость тела - физическая величина, показывающая, какое количество теплоты необходимо сообщить телу для изменения его температуры на один кельвин:
 .
.
Удельной теплоемкостью тела называется физическая величина показывающая, какое количество теплоты необходимо сообщить телу массы 1 кг для изменения его температуры на один кельвин:
 ,
,
где m – масса тела.
Молярной теплоемкостью тела называется физическая величина, показывающая, какое количество теплоты необходимо затратить для изменения температуры одного моля вещества на один кельвин:
 ,
,
где  - количество молей вещества.
- количество молей вещества.
Теплоемкость газов зависит от условий, при которых производится изменение их температуры. В зависимости от процесса изменения состояния газа теплоемкость бывает:
1. Изобарический процесс: теплоемкость при постоянном давлении  .
.
2. Изохорический процесс: теплоемкость при постоянном объеме  .
.
3. Изотермический процесс: теплоемкость бесконечно большая.
4. Адиабатический процесс: теплоемкость равна нулю.
Адиабатическим называется процесс, протекающий в системе без теплообмена с окружающей средой. К адиабатическим процессам близки все быстро протекающие процессы. Например, адиабатическим можно считать процесс распространения в упругой среде звуковых (ультразвуковых) волн.
Адиабатические процессы описываются уравнением Пуассона:
 ,
,
где g - показатель Пуассона. Показателем Пуассона называется отношение теплоемкости при постоянном давлении к теплоемкости при постоянном объеме:
 .
.
Определение величины показателя Пуассона можно производить различными методами (в частности, акустическими). В данной работе предлагается использовать для определения величины g воздуха метод адиабатического расширения воздуха.
ЭКСПЕРИМЕНТАЛЬНАЯ УСТАНОВКА. Установка для измерения g воздуха состоит из стеклянного баллона большой емкости, который при помощи крана может соединяться с насосом или атмосферой. Разность между давлением воздуха в баллоне и атмосферным давлением измеряется открытым жидкостным манометром, одно из колен которого соединяется с баллоном.
Соединив при помощи крана и резинового шланга баллон с насосом, в него нагнетают воздух. Когда разность уровней в манометре становится равной 20¸25 см, кран поворачивают до такого положения, при котором баллон будет отсоединен как от насоса, так и от окружающей среды. Процесс нагнетания воздуха в баллон происходит довольно быстро и близок к адиабатическому. Поэтому температура воздуха в баллоне увеличивается. Для установления равновесного состояния требуется некоторое время, в течение которого происходит теплообмен воздуха в баллоне с окружающей средой. При этом уровни в манометре будут перемещаться. Перемещение уровней в манометре прекратится, когда температура воздуха в баллоне станет равной комнатной температуре.
Пусть m1 -масса воздуха, находящегося в баллоне,  - абсолютная температура;
- абсолютная температура;  - давление; V - объем баллона. Очевидно, что
- давление; V - объем баллона. Очевидно, что  (если
(если  и
и  выражены в одних и тех же единицах); здесь
выражены в одних и тех же единицах); здесь  - разность уровней в манометре, соответствующая давлению
- разность уровней в манометре, соответствующая давлению  , а
, а  - атмосферное давление.
- атмосферное давление.
Определив значение  , поворотом крана соединяют воздух, находящийся в баллоне, с наружным воздухом и быстро возвращают кран в прежнее положение. В этом случае необходимо обеспечить условия, при которых процесс расширения воздуха можно считать адиабатическим, а его конечное давление - атмосферным. Точно определить момент, когда давление расширяющегося воздуха станет равным атмосферному давлению, достаточно сложно, так как после быстрого открытия крана появляются значительные колебания давления газа в баллоне. Рекомендуется возвращать кран в прежнее положение немедленно после прекращения звука, возникающего при выходе воздуха через отверстие крана.
, поворотом крана соединяют воздух, находящийся в баллоне, с наружным воздухом и быстро возвращают кран в прежнее положение. В этом случае необходимо обеспечить условия, при которых процесс расширения воздуха можно считать адиабатическим, а его конечное давление - атмосферным. Точно определить момент, когда давление расширяющегося воздуха станет равным атмосферному давлению, достаточно сложно, так как после быстрого открытия крана появляются значительные колебания давления газа в баллоне. Рекомендуется возвращать кран в прежнее положение немедленно после прекращения звука, возникающего при выходе воздуха через отверстие крана.
При адиабатическом расширении воздуха его внутренняя энергия уменьшается и, соответственно, понижается температура до значения  при давлении
при давлении  . Так как при расширении часть воздуха из баллона выйдет, масса оставшегося в баллоне воздуха будет меньше
. Так как при расширении часть воздуха из баллона выйдет, масса оставшегося в баллоне воздуха будет меньше  , обозначим ее через
, обозначим ее через 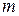 , объем по-прежнему будет
, объем по-прежнему будет  .
.
После возвращения крана в прежнее положение воздух в баллоне начинает нагреваться вследствие теплообмена с окружающей средой, давление его увеличивается, о чем можно судить по перемещению уровней в манометре. Когда температура воздуха в баллоне станет равной комнатной, перемещение уровней прекратится, их разность h2станет постоянной. Таким образом, в этом состоянии температура воздуха в баллоне равна  , а его давление
, а его давление  .
.
Рассмотрим три состояния воздуха в баллоне.
1. При давлении  и температуре
и температуре  масса воздуха
масса воздуха 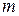 занимает объем
занимает объем  (объем
(объем  занимает масса
занимает масса  ).
).
2. При давлении  и температуре Т2 масса воздуха
и температуре Т2 масса воздуха 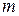 занимает объем V .
занимает объем V .
3. При давлении  и температуре Т1 масса воздуха
и температуре Т1 масса воздуха 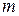 занимает объем V .
занимает объем V .
Переход из первого состояния во второе происходит адиабатически. Для него справедливо уравнение Пуассона в виде:
 . (1)
. (1)
Переход из второго состояния в третье происходит без изменения объема (изохорический процесс). Для него можно применить закон Гей-Люссака:
 . (2)
. (2)
Исключив из уравнений (1) и (2) Т1 и Т2 , получим:
 . (3)
. (3)
Логарифмируя уравнение (3), находим:
 . (4)
. (4)
Разложим  и
и  в ряд Тейлора и ограничимся двумя первыми членами (
в ряд Тейлора и ограничимся двумя первыми членами (  и
и  значительно меньше
значительно меньше  ):
):

Подставляя эти значения в (4), получим:
 . (5)
. (5)
ЗАДАНИЕ
1. Открыть кран К и накачать воздух в баллон так, чтобы разность уровней жидкости в манометре составляла 20¸25 см.
2. Закрыть кран и, выждав 2-3 минуты (до тех пор, пока уровни жидкости в трубах манометра перестанут изменяться), отсчитать по шкале уровни в левой и правой трубках манометра.
3. Быстро открыть и тотчас закрыть кран. Снова выждав 2-3 минуты, отсчитать по шкале уровни жидкости в трубках манометра.
4. Опыт проделать 7 раз. Результаты каждого измерения занести в таблицу.
Порядок проведения вычислений:
а) вычислить h1 - разность уровней до расширения;
б) вычислить h2 - разность уровней после расширения;
в) по формуле (5) вычислить gi;
г) рассчитать среднее значение  ;
;
д) вычислить погрешность каждого измерения  и абсолютную погрешность
и абсолютную погрешность  .
.
Таблица
| № | Уровни до расширения, см | h1, см | Уровни после расширения, см | h2, см | h1-h2 см | gi | gср | Dgi | Dg | ||
| левый | правый | левый | правый | ||||||||
| 1. | |||||||||||
| 2. | |||||||||||
| 3. | |||||||||||
| 4. | |||||||||||
| 5. | |||||||||||
| 6. | |||||||||||
| 7. |
Результат представить в виде:
 e = …..%.
e = …..%.
|
КОНТРОЛЬНЫЕ ВОПРОСЫ:
1. Что такое теплоемкость газа при постоянном давлении Cp и при постоянном объеме CV?
2. Дать определение адиабатического процесса. Каким уравнением описывается адиабатический процесс?
3. Как определить теоретическое значение показателя адиабаты g для азота (основного компонента воздуха)?
4. Как определяется число степеней свободы молекулы i ? Чему равно число степеней свободы для молекулы азота N2?
5. В чем заключается первое начало термодинамики?
6. Как вычисляется работа газа при адиабатическом процессе?
ЛИТЕРАТУРА:
1. Трофимова Т.И. Курс физики. М.: Высш.шк., 1985, Гл.9, §§ 50-55.
2. Савельев И.В. Курс общей физики. Кн.1. Механика·Молекулярная физика. М.: ”Наука”, 1989, Гл.10, §§ 68, 69, 72.
3. Практикум по общей физике. Под ред. проф. В.Ф.Ноздрева. М., «Просвещение», 1971, Гл.2, С.97.